自然軌道解析(NBO解析)による錯体の価数の決め方
NBOを利用する手法についての解説、第二弾です。(第一弾はこちら)
興味を持っている分子について、どんなふうに電子が分布しているか、しりたいですよね!
Mulliken電子密度は、計算化学を初めて最初に触れる電子密度についての情報だと思います。Mullken電子密度は、小さな有機物について考える場合なんかは十分なパラメータなのですが、少し重たい元素が入ってくると、問題になることも多いそうです。
興味を持っている分子について、どんなふうに電子が分布しているか、しりたいですよね!
Mulliken電子密度は、計算化学を初めて最初に触れる電子密度についての情報だと思います。Mullken電子密度は、小さな有機物について考える場合なんかは十分なパラメータなのですが、少し重たい元素が入ってくると、問題になることも多いそうです。
いにしえの頃、非常に原始的なSTOを基底関数にして計算していた時にはそれで良かったようですが、diffuse関数や、分極関数が存在する基底ではまずいそうだ。名大の計算機センターのpdfに詳しいです。
そもそも分子の中で非局在化している電子の所在は、なかなか特定しづらいものです。(だから価数なんて考えてもしゃーないやん、とか言う人もいらっしゃいます。私とは宗派が違いますが。)
ざっくりとMulliken電子密度の問題点を書くと、それぞれの原子の軌道の形などを考慮せず、結合の適当な位置にズバッと線を引いて、電子の数をカウントするところが問題です。
水素分子のような等核2原子分子ならど真ん中でOKでしょうが、C–H結合の真ん中に線をひいても、正しい価数のカウントにはなりませんよね?たとえばsp2混成の場合とsp3混成の場合で、線を引く位置は変わりそうです。
分子骨格が似た分子同士で、原子上のMuliken電子密度を比較することには使えそうですが、それ以外の用途には厳しい手法です。
私は遷移金属錯体の計算を行いますが、たとえばどっからどう見ても2価の銅錯体のテトラアンミン銅錯体のCu上に乗っかっているMulliken Chargeは +0.744 で、全然 +2 からは遠い(図1)。
図2. テトラアンミン銅(II)錯体のMulliken Charge Density
あれ、銅のアンモニア錯体は平面ちゃうの?と思ったあなたは鋭い。この計算では、カウンターアニオンや溶媒の影響を考慮していませんが、どうやら、軸位に相互作用するものがまったくない場合、少し四面体様の歪を持つみたいです。CCDCの構造検索も軽くして見ましたが、だいたい軸位に何かが弱く相互作用すると平面錯体になるようですね。
通常の分子軌道計算を行った場合と同様に、gaussian view でchkファイルを開き、赤と緑のp軌道が書かれたボタンを押すと、軌道を表示するためのウィンドウが開きます。
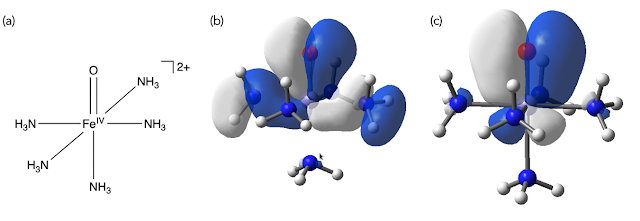
ここで、上からポチポチと軌道を可視化していき(クリックで黄色ハイライト状態にして、updateボタンを押す)、d軌道の形状を持った軌道を探します。Cu(NH3)4について計算した例では、上から5つが、d軌道に対応していました。ベータの空軌道は、4p性も大きな軌道ですが、たしかにdx2-y2の成分があることが見て取れます(図2)。
図2. テトラアンミン銅(II)錯体のNBO解析
しかし、ちょっとわかりにくいですよね。そんな場合は、Visualize, Isovalue の項目でIsovalueの値を少しずつ大きくしていくと、重要でない軌道の成分が少なくなっていき、見やすくなります。
右下の図は、まった同じ34番目のベータ軌道ですが、Isovalue を0.124としました。他の図ではIsovalueは 0.1 です。0.2くらいにすると、まったく4p成分は見えなくなります。
Isovalueの説明についてはこちら! [4/4日改訂。先日の記述は間違っていました。]
ちなみに、logファイルから、対応する軌道を探せば、その中にそれぞれ幾らの割合で、s p d が入っているかがわかります。NBOの出力の問題で、GaussViewで表示される軌道の番号と、log ファイル内の軌道の情報がシャッフルされてしまいます。
対応する軌道の情報を見つけるには、少しコツが必要で、他サイトに丁寧な説明があるので、こちらを参考にしていただければと思います。計算科学.comさん: NBO計算の可視化方法
整理すると、電子の入ったNBOが、アルファ軌道に5つ、ベータ軌道に4つあり、ベータの空軌道に、金属のd軌道性の高い軌道がある、ということがわかりました。
つまり、この銅中心はd = 9 の電子配置を取っている Cu(II) であるといえるわけです。
log ファイルを開くと、これらのd軌道は、non-bonding orbital として帰属されています。
結晶場理論では、d軌道は配位子の静電場による影響を受け、エネルギー分裂を起こしますが、ここではd軌道と配位子の軌道の間のあらわな分子軌道生成は考えません。これと似た状況を作っていると言えるでしょう。
しかし、NBO解析ではこれらの d軌道がnon-bonding として現れていることからわかるように、配位子との軌道生成の寄与が正しく反映されていません。d軌道のエネルギーの値はそのまま使えるものではないことを頭の片隅に入れておいていただければと思います。
たとえばこの解析手法は、銅(III)錯体の価数を計算化学的に議論するために利用されています (N. W. Aboelella et al. J. Am. Chem. Soc. 2002)。
この論文では、NBO解析の結果、電子の入ったd軌道が8つあることから、Cuは3価だろうと議論しています。
NBOを作る手前のNBAを利用した解析もよく用いられるようですね(PC Chem Basics.comさん: 電荷密度解析をしてみよう)。
NBOを行うには、キーワードセクションにPOP= NBOを入れればOKです。gaussian view からも、クリックだけで計算を指定できるようになっています。NBOのタブから、Type: Full NBOとして、Checkpoint Save: save NBOs としておけば、chk ファイルを読み込むと、NBOが見られるようになります。


コメント
コメントを投稿